МОЛЕКУЛЯРНАЯ ГЕНЕТИКА ДИАГНОСТИЧЕСКИХ И ПРОГНОСТИЧЕСКИХ ЭКЗАМЕНОВ ПРИ ПАРОДОНТАЛЬНОЙ БОЛЕЗНИ : Пользуясь последними технологическими инновациями в области анализа ДНК, несколько биотехнологических компаний посвятили себя разработке инновационных высокотехнологичных приложений в области отслеживания ДНК, способных обеспечить индивидуальные интегрированные решения для разработки молекулярно-генетических тестов.
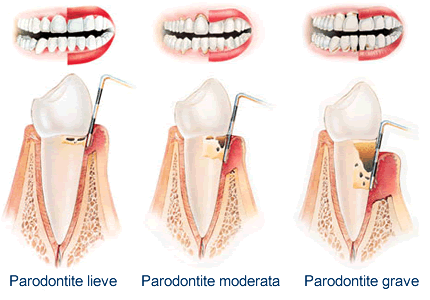
Заболевания пародонта (в его различных более или менее тяжелых формах: локализованный ювенильный пародонтит, хронический пародонтит, рефрактерный пародонтит, язвенно-некротический гингивит. Патогномоничным признаком является пародонтальный карман, который возникает, когда дегенеративный процесс выходит за пределы соединительного крепления зубного элемента. Разрушение опорных структур зуба является результатом неэффективного действия защитных систем организма в ответ на накопление микробного налета, состоящего из особых патогенных пародонтальных бактерий. Этот процесс различается как по степени, так и по тяжести у разных людей и даже у одного и того же человека.
ФАКТОРЫ РИСКА ЗАБОЛЕВАНИЙ ПАРОДОНТА
1. Генетическая конституция пациента
Риск развития пародонтита имеет четкую генетическую составляющую. В частности, часто встречающийся в популяции вариант ДНК (полиморфизм), определяющий избыточное производство медиатора воспаленияинтерлейкина 1 (IL-1)способствует чрезмерной воспалительной реакции в кости зуба и окружающей соединительной ткани, с гиперактивацией остеокластов, вызывающих агрессивную резорбцию кости. Со временем это приводит к углублению отслоения зуба от десны.
Впервые это открытие было сделано четырнадцать лет назад, когда американские генетикивпервые обратили внимание на группы пациентов, которые имели отличную гигиену полости рта и низкий процент пародонтопатогенных бактерий, но у которых, тем не менее, наблюдалась заметная деградация челюстной кости. У большинства этих пациентов был обнаружен вариант, индуцирующий избыточную продукцию IL-1, который вызывал сильный иммунный ответ в соединительной ткани и кости зуба, несмотря на присутствие небольшого количества бактерий. Последующее исследование показало, что при наличии наследственного риска вероятность развития пародонтита значительно выше. При добавлении других предрасполагающих факторов, таких как курение, плохая гигиена полости рта, системные заболевания и стресс, этот риск увеличивался в 10 раз.
Пациенты с генетической предрасположенностью к пародонтозу должны чаще проходить осмотры и соблюдать специальную домашнюю гигиену, что позволит отсрочить или избежать появления заболевания.
ПЕРИИМПЛАНТИТ. Недавние исследования, проведенные в Швейцарии и Соединенных Штатах Америки по поводу неудач при установке зубных имплантатов, показали, что курильщики, особенно те, кто имеет положительную реакцию на полиморфизм в гене IL-1, имеют высокий риск (в 3 раза выше) потери имплантатов. Проведение теста на генетическую предрасположенность перед установкой зубных имплантатов позволяет оценить риск периимплантита, который может привести к поломке имплантата; таким образом, это является гарантией безопасности как для пациента, так и для стоматолога.
2. Специфический набор видов бактерий, составляющих бляшку
Колонизация поверхности зубов бактериями признана основным этиологическим фактором развития заболеваний пародонта. Многие исследования бактерий полости рта показали, что лишь некоторые из 400 видов бактерий, упомянутых выше, обладают высокой патогенностью, что может вызвать тяжелые заболевания пародонта. Патогенные бактерии, используемые в качестве маркеров пародонтита, относятся к группе черно-пигментированных облигатно-анаэробных грамотрицательных бактерий, таких как Actinobacillus actinomycetemcomitans (также называемый Haemophilus actinomycetem-comitans), Tannerella forsythensis, Prevotella intermedia, Porphyromonas gingivalis, Treponema denticola и другие. Эти бактерии, вызывающие пародонтит, характеризуются выработкой различных метаболитов и факторов вирулентности, которые в совокупности приводят к разрушению тканей пародонта или инактивации защитных механизмов иммунной системы. В частности, высокопатогенные виды Actinobacillus actinomycetemcomitans, Porphyromonas gingivalis и Tannerella forsythensis обладают высоким спектром патогенных факторов, присутствие которых в десневых карманах может привести к потере зубов. Помимо этих высокопатогенных бактерий, существуют и другие умеренно патогенные бактерии, потенциал которых зависит от концентрации, в которой они присутствуют.
Количественный расчет соотношения между каждым пародонтопатогенным видом бактерий и общей бактериальной нагрузкой (распространенность) также дает важный диагностический показатель, посколькуActinobacillus actinomycetemcomitansчасто ассоциируется с локализованным ювенильным пародонтитом, Porphyromonas gingivalisобычно ассоциируется с хроническим периодонтитомхроническим периодонтитом, Tannerella forsythensisирефрактерным периодонтитом; а также предоставляет терапевтические рекомендации по целенаправленному и эффективному использованию конкретных антибиотиков в дозах, необходимых для уничтожения пародонтопатогенных бактерий.
3. Другие факторы
Другими факторами, предрасполагающими к развитию заболеваний пародонта, но менее значимыми, чем предыдущие, являются:
Тартар:Зубной камень представляет собой наиболее важный фактор удержания зубного налета и, следовательно, облегчает все воспалительные процессы, которые также включают выработку токсинов, участвующих в возникновении пародонтита.
Курение:Курение является экологическим фактором риска номер один для развития заболеваний пародонта, оно может вызвать рецессию десны и резорбцию костной ткани даже при отсутствии заболеваний пародонта.
Системные заболевания и лекарства:Инсулинозависимый диабет, синдром Дауна, ревматоидный артрит, ВИЧ-инфекция — это заболевания, которые делают человека более восприимчивым к пародонтозу. Такая же повышенная восприимчивость может быть вызвана применением некоторых лекарственных препаратов, таких как: стероиды, циклоспорин, оральные контрацептивы, антагонисты кальция и т.д.
Пародонтоз, который отвечает за хроническое воспаление с выбросом медиаторов воспаления в кровообращение, также является фактором риска следующих заболеваний:
ИШЕМИЧЕСКАЯ БОЛЕЗНЬ СЕРДЦА, РЕСПИРАТОРНЫЕ ЗАБОЛЕВАНИЯ, ДИАБЕТ, ПРЕЖДЕВРЕМЕННЫЕ РОДЫ И РОЖДЕНИЕ ДЕТЕЙ С НЕДОСТАТОЧНЫМ ВЕСОМ.
МОЛЕКУЛЯРНАЯ ГЕНЕТИКА ЗАБОЛЕВАНИЙ ПАРОДОНТА ДИАГНОСТИЧЕСКИЕ И ПРОГНОСТИЧЕСКИЕ ТЕСТЫ
Пользуясь последними технологическими инновациями в области анализа ДНК, несколько биотехнологических компаний посвятили себя разработке инновационных высокотехнологичных приложений в области отслеживания ДНК, способных обеспечить индивидуальные комплексные решения для разработки молекулярно-генетических тестов.
Одним из таких приложений является система PerioProfile — самый передовой на сегодняшний день подход для мониторинга развития гингивита в пародонтит и его клинического течения.
Периопрофиль— комбинированный тест, состоящий из:
1) ГЕНЕТИЧЕСКИЙ ТЕСТ, который выявляет панель4 полиморфизмовв кластере генов интерлейкина 1 и
2) МИКРОБИОЛОГИЧЕСКИЙ ТЕСТ, который включает количественное определение 5 видов пародонтопатогенных бактерий. В ходе наблюдения за пациентом необходимо повторить только микробиологический тест.
Периопрофиль основан на методе количественной ПЦР в реальном времени. В недавнем исследовании на большом количестве пациентов было обнаружено, что многие образцы, которые были отрицательными при использовании методов бактериологического анализа, применявшихся до сих пор (количественный анализ анаэробных культур), оказались положительными при использовании количественной ПЦР в реальном времени — метода молекулярной биологии, который оказался новым, высокочувствительным и специфичным инструментом, а также быстрым в использовании.
Основные преимущества анализа ПЦР в реальном времени с помощью новых инструментов, доступных сегодня, следующие:
(a) этот вид анализа является наиболее чувствительным среди методов молекулярной биологии. Использование специальных химикатов и фотоумножителей позволяет определить даже одну копию гена;
(b) позволяет проводить КАЧЕСТВЕННЫЙ анализ, давая информацию о количестве копий генов или бактериальной нагрузке образца; (c) является самым быстрым методом исследования, доступным на рынке; традиционные методы предусматривают предварительное культивирование клеточных культур, что растягивает анализ как минимум на 10-15 дней, или гибридизационные методы с гораздо более низкой чувствительностью.
В конечном итоге, благодаря инновационному методу количественной ПЦР в реальном времени, эти тесты достигают чувствительности в 10 000 раз выше, чем методы, используемые до сих пор, и достоверности результата 99, 9999% , что является самым высоким показателем, достижимым на научном уровне.
Обычные лаборатории генетического и микробиологического анализа не начинают с углубленного изучения последних данных научной литературы и использования технологически инновационных приборов, недавно появившихся на рынке, поэтому они не могут предоставить клиенту услугу по изучению и разработке индивидуальных тестов.
