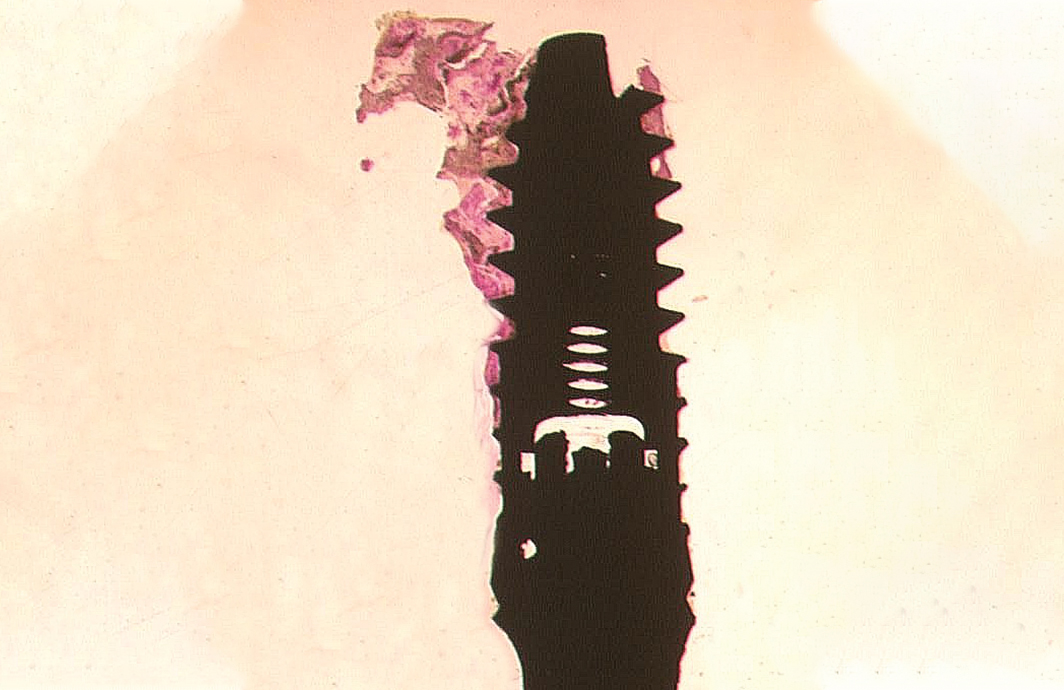
В настоящее время имплантология является одним из методов реабилитации пациентов с частичным или полным отсутствием зубов.
Позволяет восстановить как функциональность, так и эстетику на высоком уровне с предсказуемостью успеха от 90 до 95% (1).
Бактериальная инфекция может поражать только слизистую оболочку периимплантата (мукозит) (2) или также затрагивать опорную кость (периимплантит) (3).
Правильная диагностика заболеваний периимплантита необходима для правильного устранения воспалительных заболеваний.
Поддерживающая пародонтологическая терапия является ключевым моментом в сохранении здоровья полости рта пациента с имплантацией.
Один из вопросов, который должен задать оператор:
«Какие критерии следует учитывать при разработке программы поддержки, которая имеет адекватный интервал отзыва для предотвращения возможных воспалительных осложнений периимплантатных тканей?»
Исключив послеоперационные осложнения и раннюю потерю имплантата как факторы риска, мы попытаемся сосредоточиться на соответствующих диагностических параметрах заболеваний периимплантита, с целью предоставления рекомендаций, которые могут быть полезны для гигиениста стоматологического в клинической практике.
Критерии успеха имплантации были подробно описаны Альбректссоном во время первого Европейского семинара по пародонтологии в Иттингене, Швейцария, в 1993 году (4) и вкратце сводятся к следующему.
- Отсутствие мобильности.
- Отсутствие постоянных субъективных жалоб (боль, ощущение инородного тела, дизестезия).
- Отсутствие радиолюценции вокруг имплантата.
- Нет глубины кармана > 5 мм.
- Нет кровотечения при зондировании.
- После первого года нагрузки, вертикальная потеря кости не более 0, 2 мм (в нашем протоколе мы больше стремимся к поддержанию стабильных параметров, полученных в начале терапии).Давайте теперь посмотрим, каковы потенциальные факторы риска, связанные с заболеваниями периимплантита.
Нагноение
Наличие гноя является результатом инфекционно-воспалительного поражения; в исследовании, проведенном на 218 пациентах, обследованных на предмет биологических осложнений на остеоинтегрированных имплантатах в период с 9 до 14 лет, наличие гноя было определено как прогностический показатель развития периимплантита с последующей потерей уровня кости (5).
Индекс кровотечения
Наличие кровотечения при легком зондировании (0, 25N), является полезным параметром для диагностики воспаления слизистой оболочки периимплантата. Lang et al. (6) в экспериментальном исследовании показали, что здоровые периимплантиты не имели BOP, в то время как BOP увеличился в 91% мест с периимплантитом.
Прогностическое значение BOP было изучено в проспективном клиническом исследовании, оценивающем прогрессирующую потерю прикрепления у пациентов с периимплантитом (7).
Затем это было подтверждено в другом проспективном исследовании (8), в котором участки с кровотечением во время отзыва, выполненного для 2-летнего наблюдения, показали продолжающееся заболевание. Поэтому BOP считается надежным параметром для диагностики заболеваний периимплантита.
PPD и изменения в уровне клинической привязанности
Пародонтологическое зондирование является необходимым инструментом для диагностики заболеваний периимплантита. Экспериментальные исследования показали, что увеличение глубины зондирования со временем связано с потерей костного прикрепления (9).
Сила зондирования: В исследовании здоровых околоимплантатных тканей оценка сопротивления тканей зондированию околоимплантатных тканей при различных уровнях силы показала, что околоимплантатные ткани чувствительны к изменениям силы.
В прошлом высказывалось мнение, что зондирование вокруг имплантатов может привести к повреждению околоимплантатной слизистой оболочки, поэтому обычно оно не используется.
Однако Эттер и др. в экспериментальном исследовании оценили зондирование с силой 0, 25 Н и наблюдали полную реформацию слизистой через 5 дней, поэтому зондирование пародонтальным зондом с небольшим давлением 0, 25 Н не вызывает повреждения тканей периимплантата и рекомендуется для их оценки (10).
Анализ слюны и щелевой жидкости
Корреляция между биохимическими маркерами воспаления и клиническими параметрами здоровых и больных периимплантитных тканей была в центре внимания последних исследований.
Уровень биохимических медиаторов, выделяемых в PICF (периимплантной щелевой жидкости), был изучен с целью выявления диагностического маркера для мониторинга здоровья периимплантов.
Были изучены маркеры ПИКФ, включая цитокины, ферменты и протеазы.
Совсем недавно оценивались образцы слюны, преимущество которых в том, что они неинвазивны и их легче собирать, чем ПЦИФ.
В то время как эти тесты указывают на потенциал для диагностического тестирования, для периимплантита существует необходимость в проспективных продольных исследованиях для корреляции прогрессирования заболевания с биохимическими маркерами.
Продолжаются исследования в поисках чувствительного диагностического теста для выявления обратимых изменений до клинических изменений периимплантита, однако на сегодняшний день не существует биохимического диагностического теста для выявления прогрессирования периодонтита.
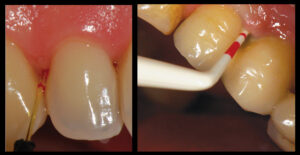
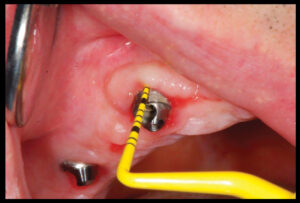
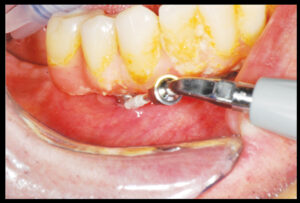
Микробиологический диагностический тест
Luterbacher и др. оценили микробиологический тест в сочетании с BOP для мониторинга состояния тканей вокруг имплантата в течение 2-летнего периода наблюдения.
Во время каждого контрольного посещения брался микробиологический образец в месте установки имплантата и зуба для определения наличия специфических бактерий (Aggregatibacter actinomycetemcomitans, Prevotella intermedia, Porphiromonas gingivalis и Treponema denticola), также регистрировалось наличие или отсутствие BOP (8).
В период последующего наблюдения был рассчитан процент визитов по отзыву с положительными бактериологическими тестами и позитивностью BOP.
Глубина зондирования периимплантов контролировалась для выявления прогрессирования заболевания периимплантов.
Сообщалось, что добавление результатов микробиологических исследований повышает прогностическую значимость только BOP в определении прогрессирования заболевания на уровне имплантатов.
Рентгенографическая оценка
Рентгенографические методы, включая ортопантомографию и внутриротовую рентгенографию с использованием метода параллельного луча, широко используются для мониторинга краевых уровней кости на имплантатах и диагностики потери межпроксимальной кости.
Расстояние от фиксированной точки отсчета до уровня интерпроксимальной кости регистрируется и отслеживается в продольном направлении.
Хотя ортопантомография обеспечивает обзор имплантатов, существуют ограничения, включая разрешение и искажение самого изображения.
К другим ограничениям обычной рентгенографии относится невозможность контролировать уровень вестибулярной и язычной/палатальной кости, низкая чувствительность к раннему выявлению изменений кости и недооценка степени потери костной ткани.
Использование компьютерного анализа изображений может повысить диагностическую точность рентгеновских снимков за счет выявления небольших изменений плотности костной ткани.
Томография является наиболее широко используемым методом исследования в реабилитации на имплантатах, предлагая преимущество представления костных структур в 3 плоскостях в полном масштабе и без искажений.
Менгель и др. в экспериментальном исследовании на нижней челюсти свиньи оценили точность и качество отображения периимплантатных дефектов с помощью внутриротовой рентгенографии, панорамной рентгенографии, КТ и техники параллельного луча.
Как КТ, так и метод параллельного луча обеспечивают точное трехмерное изображение периимплантатных костных дефектов (11).
Диабет
Диабет — это системное заболевание, которое является результатом бесчисленных механизмов, способных задерживать заживление ран, тем самым повышая восприимчивость пациента к инфекции или потере имплантата (12).
Существует только одно исследование, описывающее связь между диабетом и периимплантитом: в 2006 году Феррейра и др. в кросс-секционном исследовании 212 некурящих людей показали, что плохой метаболический контроль у людей с диабетом связан с заболеванием периимплантита.
Генетика
Интерлейкин1α, IL1β и их специфические ингибиторы воспаления IL-1ra играют ключевую роль в регуляции воспалительного ответа.
Выявление полиморфизма генов при периимплантной инфекции было исследовано в нескольких клинических испытаниях с противоречивыми результатами.
В недавнем обзоре была предпринята попытка выяснить, существует ли ассоциация между положительным интерлейкином-1 и повышенной потерей костной ткани около имплантатов. Из анализа 44 научно значимых публикаций только 2 исследования оказались значимыми, что свидетельствует о наличии доказательств в пользу ассоциации между статусом курения IL- 1+ и развитием периимплантита.
Кроме того, была продемонстрирована более высокая частота заболеваний периимплантита у пациентов, которые курят IL-1+ (13).
Влияние курения сигарет на ткани периимплантита было зафиксировано в многочисленных исследованиях.
Штритцель и др. опубликовали мета-анализ, чтобы выяснить, влияет ли курение на прогноз имплантации. Поскольку определение курильщика в разных исследованиях было различным (по количеству выкуриваемых сигарет в день), в данном обзоре курильщиком считался каждый пациент, который курил.
Данный обзор существенно указывает на риск биологических осложнений у курильщиков по сравнению с некурящими.
В некоторых исследованиях, включенных в данный обзор, сообщалось о частоте заболеваний периимплантита, усилении воспаления, нагноении, образовании свищей, периимплантите, потере костной ткани, высокой частоте кровотечений, воспалении слизистой периимплантита.
В этот обзор также включены исследования о влиянии курения на изменения краевой кости периимплантов, которые показали значительное увеличение потери краевой кости у курильщиков по сравнению с некурящими (13).
Дальнейшие исследования показали, что потеря костной ткани около имплантатов связана с привычным потреблением сигарет.
TPS у пациентов с имплантатами во время средне- и долгосрочного наблюдения
Как уже упоминалось ранее, факторы риска могут способствовать развитию периимплантологических патологий по отдельности или совместно, что обусловливает необходимость их контроля и мониторинга.
Клинические данные заставили нас также учитывать тип протеза, изготовленного во время реабилитации.
Выбор включения «типа протеза» в факторы риска в протоколе мотивирован наблюдением, что в клинической практике различные типы протезов могут влиять на правильную домашнюю гигиену полости рта пациента при имплантации.
На самом деле, у пациента могут быть объективные трудности с удалением мягких отложений с протезных конструкций.
Структура, а иногда и сложность проекта протезирования может представлять реальную трудность в управлении для пациента, мешая ему достичь оптимального уровня гигиены полости рта в домашних условиях.
Таким образом, наличие «трудноудаляемого» налета может способствовать, в дополнение к вышеупомянутым факторам риска, возникновению заболевания околоимплантатной ткани.
Протокол
В Университетском центре гигиены и профилактики полости рта больницы Сан-Раффаэле в Милане был разработан протокол для оценки факторов риска, которые могут способствовать этиопатогенезу заболеваний периимплантита, таких как
- тип изготовленного протеза,
- курение;
- домашняя гигиена полости рта;
- предшествующая пародонтопатия;
- диабет
В протоколе переменный тип протеза, изготовленного при имплантопротезной терапии, был включен в число факторов риска, поскольку в клинической практике различные типы протезов могут влиять на контроль правильной домашней гигиены полости рта пациента с опорой на имплантаты.
Пациент может испытывать объективные трудности при удалении мягких отложений с протезных конструкций.
Архитектура, а иногда и сложность проекта протезирования может представлять для пациента настоящую управленческую трудность, мешая ему достичь оптимального уровня гигиены полости рта в домашних условиях.
Таким образом, наличие «трудноудаляемого» налета может способствовать, наряду с ранее упомянутыми факторами риска, возникновению патологий, затрагивающих периимплантатные ткани.
После оценки здоровья периимплантатных тканей пациент вносится в протокол путем расчета профиля риска.
Метод расчета риска
Данный метод определения риска основан на оценке 5 вышеописанных факторов/показателей риска, коррелирующих с возникновением периимплантитных заболеваний. Каждому фактору/показателю присвоен балл, свидетельствующий о важности влияния данного фактора/показателя на уровень риска возникновения периимплантитных патологий (табл. 1, 2, 3, 4 и 5).
1a. Тип несъемного протеза, изготовленного при имплантопротезной терапии
| Одиночная коронка | Мост | Циркулярный | Циркулярный с ложными деснами | Протез Торонто |
|---|---|---|---|---|
| Риск | Риск | Риск | Риск | Риск |
| Точка 0 | Точка 1 | Точка 2 | Баллы 3 | Баллы 4 |
Таблица 1 Расчет риска, связанного с типом несъемного протеза
1b. Тип съемного протеза, изготовленного при имплантопротезной терапии
| Накладные зубы |
|---|
| на яйцевидные сферы |
| на телескопическую штангу/ |
| Двойная структура |
| Риск Риск Риск |
| Баллы 4 Баллы 5 Баллы 6 |
Импортировано путем ручной вставки
2. Дым
| Накладки на шары | Накладки на штангу | Телескопическая/двойная конструкция |
|---|---|---|
| Риск | Риск | Риск |
| Баллы 4 | Баллы 5 | Баллы 6 |
Таблица 2 Расчет риска, связанного с типом съемного протеза
3. Домашняя гигиена полости рта
| Некурящий | 1/9 сигарет в день | 10/19 сигарет в день | 20 и более сигарет в день |
|---|---|---|---|
| Риск | Риск | Риск | Риск |
| Баллы 0 | Баллы 1 | Баллы 2 | Баллы 3 |
Таблица 3 Расчет риска, связанного с воздействием сигаретного дыма
4. Наличие предшествующего заболевания пародонта
| =75% | |||
|---|---|---|---|
| Риск | Риск | Риск | Риск |
| Баллы 0 | Баллы 1 | Баллы 2 | Баллы 3 |
Таблица 4 Расчет риска, связанного с уходом за полостью рта на дому (IP)
Для получения общего значения, приходящегося на индивидуальный уровень риска, баллы каждого фактора риска/показателя должны быть впоследствии суммированы (табл. 6).
5. Диабет
| Да | Нет |
|---|---|
| Риск | Риск |
| Баллы 1 | Баллы 0 |
Таблица 5 Расчет риска, связанного с заболеваниями пародонта в прошлом
Расчет индивидуального уровня риска и интервала технического обслуживания
После присвоения баллов по каждому из рассматриваемых факторов/показателей риска выводится алгебраическая сумма индивидуальных баллов (табл. 7), в результате чего получается окончательный подсчет.
Общее количество: профиль риска
| Недиабетик | Диабетик с достаточной метаболической компенсацией | Диабетик с недостаточной метаболической компенсацией |
|---|---|---|
| Риск | Риск | Риск |
| Баллы 0 | Баллы 1 | Баллы 2 |
Таблица 6 Расчет риска на основе сывороточной концентрации гликозилированного гемоглобина (HbA1c).
Полученный итоговый балл позволяет назначить индивидуальный уровень риска для конкретного пациента.
Окончательные общие уровни риска подразделяются путем присвоения каждому классу риска следующих значений:
НИЗКИЙ: от 0 до 5 баллов
СРЕДНИЙ: от 6 до 10 баллов
ВЫСОКИЙ: от 11 до 15 баллов
Конкретный профилактический и терапевтический протокол ассоциируется с полученным уровнем риска с учетом временной детерминанты (табл. 8).


Затем к назначенному профилю риска применяются следующие профилактические/терапевтические протоколы.
Низкий риск
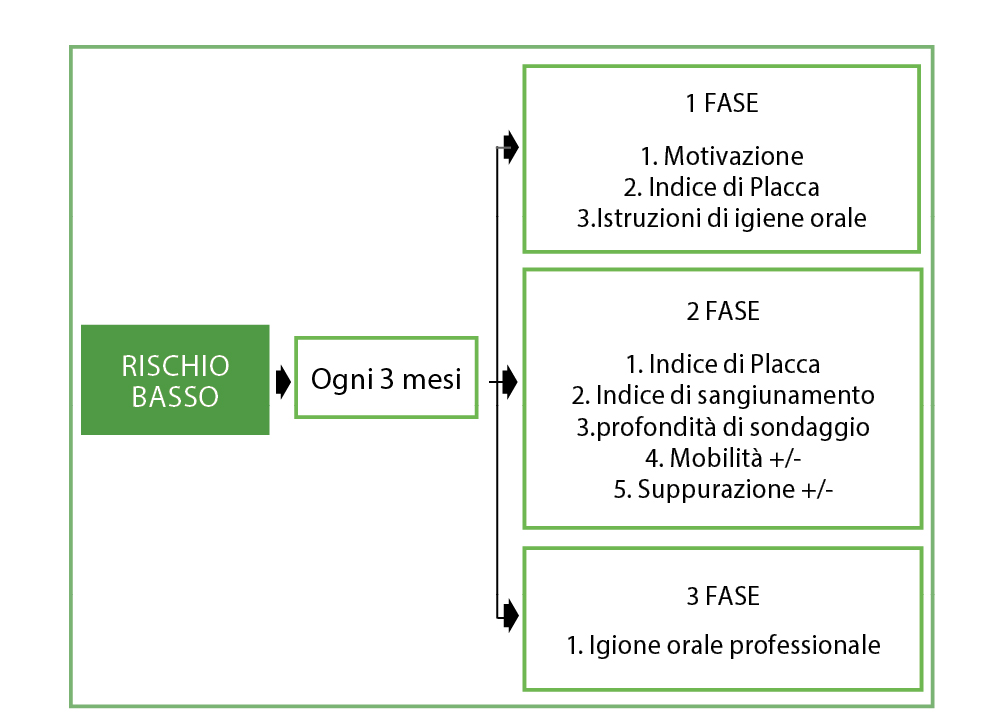 Интервал поддержания и сопутствующая терапия для низкого риска
Интервал поддержания и сопутствующая терапия для низкого риска
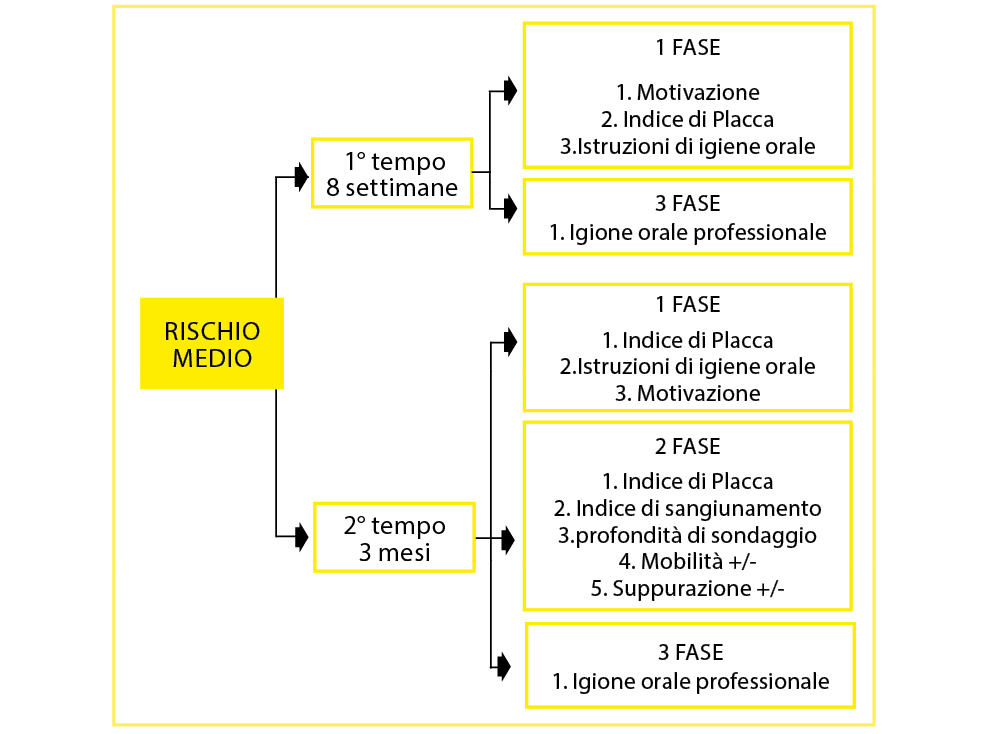
Средний риск
Пациент с профилем среднего риска будет соблюдать поддерживающий интервал, разделенный на 2 РАЗА (табл. 10).
Высокий риск
Пациент с высоким профилем риска будет соблюдать поддерживающий интервал, разделенный на 3 ВРЕМЕНИ (табл. 11).
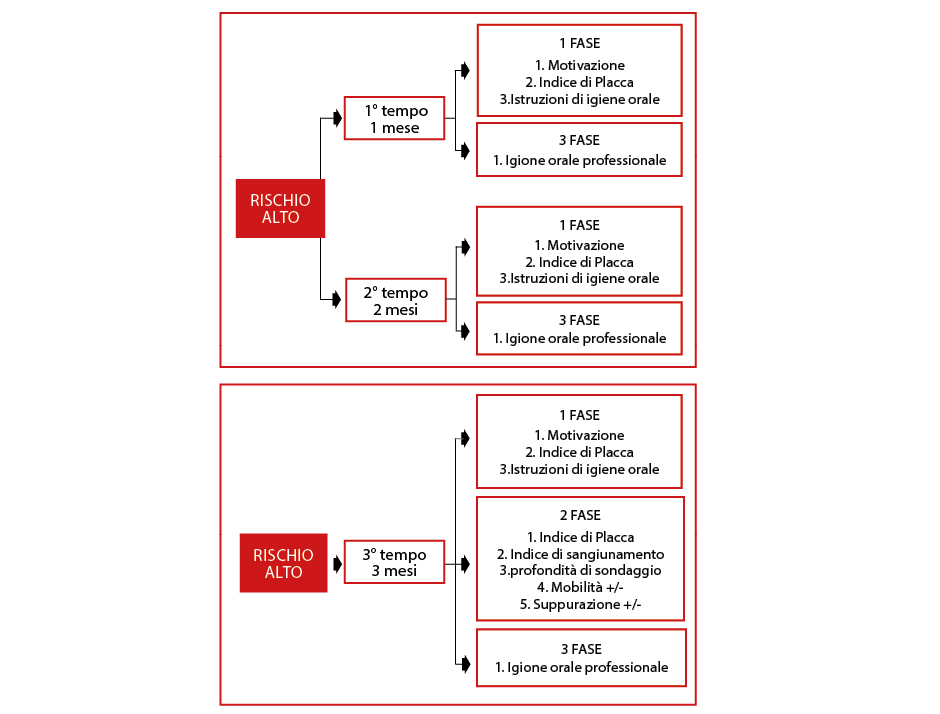 Интервал поддержания и соответствующая терапия высокого риска.
Интервал поддержания и соответствующая терапия высокого риска.
